��һ�όW(xu��)�ڻ��W(xu��)����߀ԭ����(y��ng)��(w��n)�}�������Y(ji��)
2019-01-11 21:04:41���þW(w��ng)
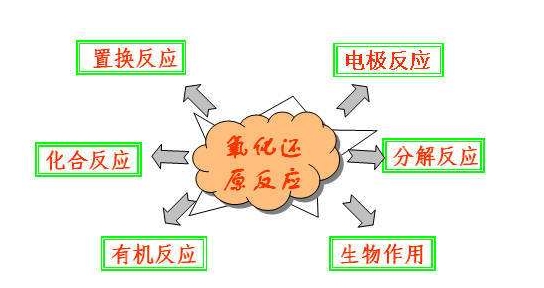
����һ������߀ԭ����(y��ng)������֮�g���P(gu��n)ϵ
����1������(y��ng)�(l��i)�ͣ�
������������(y��ng)�����|(zh��)����Ԫ�ػ��σr(ji��)���ߵķ���(y��ng)��
����߀ԭ����(y��ng)�����|(zh��)����Ԫ�ػ��σr(ji��)���͵ķ���(y��ng)��
��������߀ԭ����(y��ng)����Ԫ�ػ��σr(ji��)���ߺͽ��͵ķ���(y��ng)��
����2������(y��ng)�
�������������ڷ���(y��ng)�еõ���ӵ����|(zh��)
����߀ԭ�����ڷ���(y��ng)��ʧȥ��ӵ����|(zh��)
����3���a(ch��n)�
���������a(ch��n)�ʧ��ӱ�������õ��Įa(ch��n)��
����߀ԭ�a(ch��n)�����ӱ�߀ԭ��õ��Įa(ch��n)��
����4�����|(zh��)���|(zh��)��
���������ԣ������������F(xi��n)������ӵ����|(zh��)
����߀ԭ�ԣ�߀ԭ�������F(xi��n)��ʧ��ӵ����|(zh��)
����5������(g��)����֮�g���P(gu��n)ϵ���D
���������}1������׃���^(gu��)�̌���߀ԭ����(y��ng)����( )
����A. HCl→MgCl2
����B. Na→Na+
����C. CO→CO2
����D. Fe3+→Fe
���������}2�����л��W(xu��)����(y��ng)����������߀ԭ����(y��ng)����( )
����A.3Cl2 + 6KOH =5KCl + KClO3 + 3H2O
����B.2NO2+ 2NaOH =NaNO3 +NaNO2 +H2O
����C.SnCl4+ 2H2O = SnO2 + 4HCl
����D.3CCl4+ 2K2Cr2O7 = 2CrO2Cl2 +3COCl2 +2KCl
�����𰸣������}1��D�������}2��C
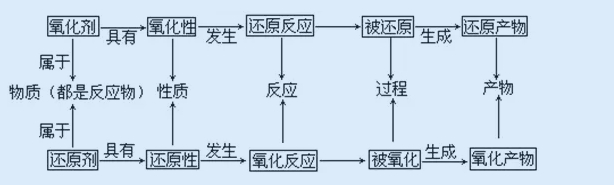
����������Ҋ(ji��n)���������c߀ԭ��
����1�����|(zh��)�ڷ���(y��ng)��������������߀������߀ԭ������Ҫȡ�Q��Ԫ�صĻ��σr(ji��)��
������1��Ԫ��̎����߃r(ji��)�r(sh��)������ԭ��ֻ�ܵõ���ӣ����ԓԪ��ֻ��������������+7�r(ji��)��Mn��+6�r(ji��)��S
������2��Ԫ��̎�����g�r(ji��)�B(t��i)�r(sh��)������ԭ���S����(y��ng)�l����ͬ�����ܵ���ӣ�����ʧ��ӣ����ԓԪ�ؼ�������������������߀ԭ������0�r(ji��)��S��+4�r(ji��)��S
������3��Ԫ��̎����̓r(ji��)�r(sh��)������ԭ�ӄtֻ��ʧȥ��ӣ����ԓԪ��ֻ����߀ԭ������-2�r(ji��)��S
����2����Ҫ��������
������1����ǽ��ن��|(zh��)����F2��Cl2��Br2��O2�ȡ�
������2��Ԫ��̎�ڸ߃r(ji��)�r(sh��)��������߃r(ji��)�����ἰ�߃r(ji��)���������}�ȣ���MnO2��NO2����H2SO4��HNO3��KMnO4��KClO3��F(xi��n)eCl3�ȡ�
������3���^(gu��)�������Na2O2��H2O2�ȡ�
����3����Ҫ��߀ԭ��
������1�����ن��|(zh��)����Na��K��Zn��F(xi��n)e�ȡ�
������2��ijЩ�ǽ��ن��|(zh��)����H2��C��Si�ȡ�
������3��Ԫ��̎�ڵͻ��σr(ji��)�r(sh��)���������CO��SO2�ȡ�
������4��Ԫ��̎�ڵͻ��σr(ji��)�r(sh��)���ᣬ��HCl���⣩��HBr��HI��H2S�ȡ�
������5��Ԫ��̎�ڵͻ��σr(ji��)�r(sh��)���}����Na2SO3��F(xi��n)eSO4�ȡ�
������������D(zhu��n)�Ƶı�ʾ����
��������D(zhu��n)�Ƶı�ʾ�������p��(xi��n)�͆ξ�(xi��n)��
����1���p��(xi��n)��
����Ҫ�c(di��n)��
������1�����^�ɷ���(y��ng)���л��σr(ji��)׃��Ԫ��ָ���������л��σr(ji��)�ѽ�(j��ng)׃���˵�ͬһԪ�ء������ߡ�����һ�����^��Խ�^(gu��)����ʽ���g�ĵ�̖(h��o)��
������2������D(zhu��n)�Ɣ�(sh��)Ŀ�����σr(ji��)���ߡ�ʧ��ӣ����σr(ji��)���͡�����ӡ����σr(ji��)��׃?c��)��ص�ԭ�ӂ�(g��)��(sh��)m×ÿ��(g��)ԭ�ӵõ�����ʧȥ����ӵĂ�(g��)��(sh��)ne-����m×ne-���磺

����2���ξ�(xi��n)��
����Ҫ�c(di��n)��
������1����(xi��n)��ķ���(y��ng)���л��σr(ji��)���ߵ�Ԫ�س��l(f��)��ָ��(y��ng)���л��σr(ji��)���͵�Ԫ�أ����^��(du��)��(zh��n)�������л��σr(ji��)���͵�Ԫ�أ����^���^(gu��)“=”
������2���ھ�(xi��n)���Ϙ�(bi��o)���D(zhu��n)����ӿ���(sh��)������(xi��)�õ���ʧȥ���磺
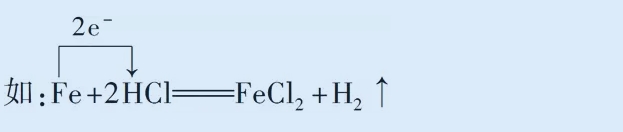
�����ġ�����߀ԭ����(y��ng)�ķ���(y��ng)Ҏ(gu��)��
����1���r(ji��)�B(t��i)Ҏ(gu��)��
����ͬ�NԪ�أ�̎����߃r(ji��)�B(t��i)�r(sh��)ֻ���������ԡ�̎����̓r(ji��)�B(t��i)�r(sh��)ֻ����߀ԭ�ԡ�̎�����g�r(ji��)�B(t��i)�r(sh��)��������������߀ԭ�ԡ�
���������}��������������߀ԭ�Ե��ǣ� ��
����A. K
����B. Fe2+
����C. S2-
����D. Na+
�����𰸣�D
����2���绯�͚w��Ҏ(gu��)��
�����r(ji��)�B(t��i)�w��Ҏ(gu��)�ɣ�ͬ�NԪ�ز�ͬ�r(ji��)�B(t��i)֮�g�l(f��)������߀ԭ����(y��ng)�r(sh��)���r(ji��)�B(t��i)��׃��“ֻ���n�����ཻ�������”��
����3������(y��ng)�Ⱥ�Ҏ(gu��)��
�����ڝ���������Һ�У�
������1��ͬ�r(sh��)���м���߀ԭ���r(sh��)��������������߀ԭ�ԏ�(qi��ng)�ă�(y��u)�ȱ�������
������2��ͬ�r(sh��)���м����������r(sh��)������߀ԭ���������ԏ�(qi��ng)�ă�(y��u)�ȱ�߀ԭ��
����4���غ�Ҏ(gu��)��
�������κ�����߀ԭ����(y��ng)�У����σr(ji��)���߿���(sh��) = ���σr(ji��)���Ϳ���(sh��)��߀ԭ��ʧ��ӿ���(sh��) = ����������ӿ���(sh��)�����ҷ���(y��ng)ǰ��늺ɔ�(sh��)��ȡ�
���������}����֪3��(g��)SO32-ǡ�Ì�2��(g��)ClO4-߀ԭ����SO32-��������SO42-���tXԪ����߀ԭ�a(ch��n)���еĻ��σr(ji��)�ǣ� ��
����A. +1
����B��+2
����C��+3
����D��+4
�����𰸣�D
�����塢�������c߀ԭ�Եď�(qi��ng)���Д�Ҏ(gu��)��
����1������(j��)����߀ԭ����(y��ng)����ʽ���Д�
���������ԣ��������������a(ch��n)��
����߀ԭ�ԣ�߀ԭ����߀ԭ�a(ch��n)��
�����ɿ��Y(ji��)�飺��ʲô�ԣ���ʲô�����a(ch��n)��֮�����ڄ���
����2������(j��)���ٻ��(d��ng)������Д�
����K Ca Na Mg AlZn Fe Sn Pb (H) Cu Hg Ag Pt Au
������������߀ԭ����u�p������(du��)��(y��ng)�x�ӵ���������u����(qi��ng)
����3������(j��)����(y��ng)�l���ͷ���(y��ng)�Ą��ҳ̶�
��������(y��ng)�l��Ҫ��Խ�ͣ�����(y��ng)Խ���ң���(du��)��(y��ng)���|(zh��)�������Ի�߀ԭ��Խ��(qi��ng)��
����4������(j��)������߀ԭ����(y��ng)�ij̶�
������ͬ�l���£�
������1����ͬ������������ͬһ�N߀ԭ���������a(ch��n)��r(ji��)�B(t��i)�ߵ������ԏ�(qi��ng)��
������2����ͬ߀ԭ��������ͬһ�N��������߀ԭ�a(ch��n)��r(ji��)�B(t��i)�͵�߀ԭ�ԏ�(qi��ng)��
������������߀ԭ����(y��ng)����ʽ����ƽ
����1������(g��)ԭ�t����ʧ����غ�ԭ�t��ԭ���غ�ԭ�t��늺��غ�ԭ�t
����2��һ�㷽�������σr(ji��)������(li��n)����С������(sh��)��
����3����ƽ���ɣ�
������1��������ƽ�����ȏ���������߀ԭ���_(k��i)ʼ��ƽ��
�����m�÷����������g������߀ԭ����(y��ng)������Ԫ���c������߀ԭ����(y��ng)�������������|(zh��)��������������߀ԭ�a(ch��n)�
������2��������ƽ�����ȏ�����߀ԭ�a(ch��n)���_(k��i)ʼ��ƽ��
�����m�÷�������������߀ԭ����(y��ng)������(y��ng)����ijһ���ֱ�������߀ԭ
������3�����w��ƽ�l(f��)����(d��ng)ijһԪ�ص�ԭ�ӻ�ԭ�ӈF(tu��n)����Ҋ(ji��n)���ЙC(j��)����(y��ng)��ƽ����ij���������Д�(sh��)��(g��)�r(sh��)���Ɍ�������һ��(g��)���w��(du��)��������(j��)��������Ԫ�ػ��σr(ji��)����(sh��)�͞����ԭ�t�������w��(bi��o)�r(ji��)��
������4��ȱ�(xi��ng)��ƽ��
����������o�Ļ��W(xu��)����ʽ���з���(y��ng)���������](m��i)�Ќ�(xi��)����(l��i)������ƽ�r(sh��)���������ȱ�����|(zh��)���l(f��)����ӵĵ�ʧ���H�H���ṩһ�N�l(f��)������(y��ng)���ᡢ�A�����Եĭh(hu��n)�������Ȱ��л��σr(ji��)������Ԫ����ƽ��������(j��)늺��غ��ԭ���غ�_��ȱ�(xi��ng)���|(zh��)����ƽ��
���������}��BiO3���� Mn2���� =Bi3���� MnO4���� H2O
�������������ȸ���(j��)���σr(ji��)��������ƽ��׃�r(ji��)Ԫ�ص����P(gu��n)���|(zh��)��
����5BiO3����2 Mn2���� =5Bi3����2 MnO4����H2O
��������(j��)��ԭ���غ㣬���Դ_��H2O��ϵ��(sh��)��7������(j��)�|(zh��)���غ��늺��غ�Ҏ(gu��)�ɿ��Դ_������(y��ng)����ȱ���ǚ��x��H��
������5��������ƽ��
��������ż��ƽ��
�����@�N�����m���ڻ��W(xu��)����ʽ��߅ijһԪ�ض�γ��F(xi��n)�����҃�߅��ԓԪ��ԭ�ӿ���(sh��)��һ��һż�����磺C2H2+O2→CO2+H2O��
�����˷���ʽ��ƽ���ȳ��F(xi��n)�Δ�(sh��)������ԭ������
����O2��(n��i)��2��(g��)��ԭ�ӣ��o(w��)Փ���W(xu��)ʽǰϵ��(sh��)��ף���ԭ�ӿ���(sh��)��(y��ng)��ż��(sh��)������߅H2O��ϵ��(sh��)��(y��ng)��2�����Ƴ������ķ���ϵ��(sh��)���F(xi��n)��?j��n)?sh��)�t����4�����ɴ���֪C2H2ǰ2��ʽ��׃?y��u)�?C2H2+O2→CO2+2H2O���ɴ˿�֪CO2ǰϵ��(sh��)��(y��ng)��4���������|(zh��)O2��5���Ѷ̾�(xi��n)�Ğ��̖(h��o)����(xi��)���l�����ɣ�2C2H2+5O2==4CO2+2H2O��
�������^�취��ƽ
�����Еr(sh��)����ʽ�Е�(hu��)���F(xi��n)һ�N���W(xu��)ʽ���^��(f��)�s�����|(zh��)���҂���ͨ�^(gu��)�@��(g��)��(f��)�s�ķ���ȥ���������W(xu��)ʽ��ϵ��(sh��)�����磺Fe+H2O——Fe3O4+H2��
����Fe3O4���W(xu��)ʽ�^��(f��)�s���@Ȼ��F(xi��n)e3O4��Fe��(l��i)Դ�چ��|(zh��)Fe��O��(l��i)����H2O���tFeǰ��3��H2Oǰ��4���tʽ�Ӟ飺3Fe+4H2O��Fe3O4+H2���ɴ��Ƴ�H2ϵ��(sh��)��4����(xi��)���l�����̾�(xi��n)�Ğ��̖(h��o)���ɣ�3Fe+4H2O==Fe3O4+4H2��
�����ۚwһ��
�����ҵ����W(xu��)����ʽ���P(gu��n)�I�Ļ��W(xu��)ʽ�����仯�W(xu��)ʽǰӋ(j��)����(sh��)��1��Ȼ�����(j��)�P(gu��n)�I���W(xu��)ʽȥ��ƽ�������W(xu��)ʽǰ�Ļ��W(xu��)Ӌ(j��)����(sh��)�������F(xi��n)Ӌ(j��)����(sh��)���?j��n)?sh��)���ٌ���Ӌ(j��)����(sh��)ͬ����ͬһ����(sh��)������?j��n)?sh��)������(sh��)���@�N�ȶ��P(gu��n)�I���W(xu��)ʽӋ(j��)����(sh��)��1����ƽ�������Q(ch��ng)��wһ����
�����������x�W(xu��)����ʽ�нM�����(f��)�s�Ļ��W(xu��)ʽ���O(sh��)����ϵ��(sh��)��1���������Ɣࡣ
�����ߡ�����߀ԭ����(y��ng)�����P(gu��n)Ӌ(j��)�㣨�e���f(shu��)����������2��(g��)���ӣ�
����1��Ӌ(j��)������(j��)���������õ�����ӿ���(sh��)����߀ԭ��ʧȥ����ӿ���(sh��)��
����2��Ӌ(j��)�㹫ʽ�������������|(zh��)����×׃�r(ji��)Ԫ��ԭ�ӵĂ�(g��)��(sh��)×���σr(ji��)��׃��ֵ��=߀ԭ�������|(zh��)����×׃�r(ji��)Ԫ��ԭ�ӵĂ�(g��)��(sh��)×���σr(ji��)��׃��ֵ��
���������}1��ClO2��һ�N��������Ч�ʸߡ�������ȾС��ˮ̎�턩����(sh��)�(y��n)�ҿ���ͨ�^(gu��)���·���(y��ng)�Ƶ�ClO2������(y��ng)����ʽ��2KClO3��H2C2O4��H2SO4==�ӟ�==2ClO2↑��K2SO4��2CO2↑��2H2O�������f(shu��)�����_���ǣ� ��
����A��KClO3�ڷ���(y��ng)�еõ����
����B��ClO2�������a(ch��n)��
����C��H2C2O4�ڷ���(y��ng)�б�߀ԭ
����D��1molKClO3���ӷ���(y��ng)��2mol����D(zhu��n)��
�����𰸣�A
�����������ɷ���(y��ng)����ʽ֪��KClO3��ClԪ�ػ��σr(ji��)�ɣ�5→��4��H2C2O4��̼Ԫ�صĻ��σr(ji��)�ɣ�3→��4����KClO3����ӣ�������������߀ԭ��߀ԭ�a(ch��n)��ClO2��1molKClO3���ӷ���(y��ng)�D(zhu��n)��1mol��ӣ�H2C2O4��߀ԭ������������A�(xi��ng)���_��
���������}2����11.2g��Mg��Cu�Ļ������ȫ�ܽ��������������У��ռ�����(y��ng)�a(ch��n)���Ě��wX������������Һ�м����m����NaOH��Һ���a(ch��n)��21.4g����������(j��)�}���Ɣ����wX�ijɷֿ����ǣ� ��
����A.0.3mol NO2��0.3mol NO
����B. 0.2mol NO2��0.1molN2O4
����C. 0.1mol NO��0.2mol NO2��0.05mol N2O4
����D. 0.6mol NO
�����𰸣�C
��������������(j��)Mg��Cu��׃����Mg��Mg2+��2OH����Mg(OH)2��2e����Cu��Cu2+��2OH����Cu(OH)2��2e��֪���ӵ��|(zh��)����OH�����|(zh��)�����D(zhu��n)����ӵ����|(zh��)�����cOH�������|(zh��)������ȣ��t��n(OH��)��21.4g��11.2 g/17g·mol��1��0.6 mol���ʷ���(y��ng)�D(zhu��n)�Ƶ���ӵ����|(zh��)����Ҳ��0.6mol��
�����x�(xi��ng)A�D(zhu��n)����ӵ����|(zh��)������0.3mol×1+0.3mol×3 ��1.2 mol�������_���x�(xi��ng)B�D(zhu��n)����ӵ����|(zh��)������0.2mol×1+0.1mol×2 ��0.4 mol�������_���x�(xi��ng)C�D(zhu��n)����ӵ����|(zh��)������0.1mol×3+0.2mol×1+ 0.05mol×2 �� 0.6 mol�����_���x�(xi��ng)D�D(zhu��n)����ӵ����|(zh��)������0.6mol×3��1.8mol�������_.
���������}3�������~�cһ���������ᷴ��(y��ng)�õ������~��Һ��NO2��N2O4��NO�Ļ�Ϛ��w���@Щ���w�c1.68LO2����(bi��o)��(zh��n)��r����Ϻ�ͨ��ˮ�У����К��w��ȫ��ˮ�����������ᡣ�������������~��Һ�м���5mol/LNaOH��Һ��Cu2+ǡ����ȫ�������t����NaOH��Һ���w�e�ǣ� ��
����A.60mL
����B.45mL
����C.30mL
����D.15mL
�����𰸣�A
�������������}������߀ԭ����(y��ng)�Ќ����B�m(x��)����(y��ng)���@�(l��i)�}����Ӌ(j��)���^(gu��)����ֻ�迼�]ʼĩԪ�ػ��σr(ji��)��׃����������(g��)�^(gu��)���ஔ(d��ng)��Cu��ʧȥ��ӣ�O2�ڵõ���ӡ�Cu���σr(ji��)����2��(g��)��O�Ļ��σr(ji��)���̓ɂ�(g��)���t��
����n��Cu��×1×��2-0��=n��O2��×2×��0������2����
������n��Cu��=0.15mol
��������(j��)���W(xu��)ʽCu��NO3��2����֪n��NO3-��=0.15mol×2������NaOH��Һ��NO3-��K�cNa+�Y(ji��)�ϣ�����n��Na+��=n��NO3-��=0.3mol���M(j��n)���������5mol/LNaOH��Һ���w�e��60mL��














